Gerelateerd artikel
ChIP-Seq Probleemoplossing 101: Stap voor stap Oplossen van Laag Signaal
2026-02-28ChIP-Seq Troubleshooting begint vaak met één eenvoudig symptoom—laag signaal—maar de werkelijke oorzaken zijn meestal verspreid over chromatinekwaliteit, antilichaamprestaties, immunoprecipitatiecondities en bibliotheek-QC. Bij Longlight Technology ondersteunen we labs die ChIP-Seq uitvoeren voor histonmarkeringen en transcriptiefactoren, en we zien dezelfde "stille faalpunten" zich herhalen bij verschillende instrumenten en monstertypen. Deze ChIP-Seq Troubleshooting 101-gids leidt beginners stapsgewijs door een pad om het signaal logisch te herstellen, met behulp van praktische checkpoints die je in één keer kunt verifiëren.
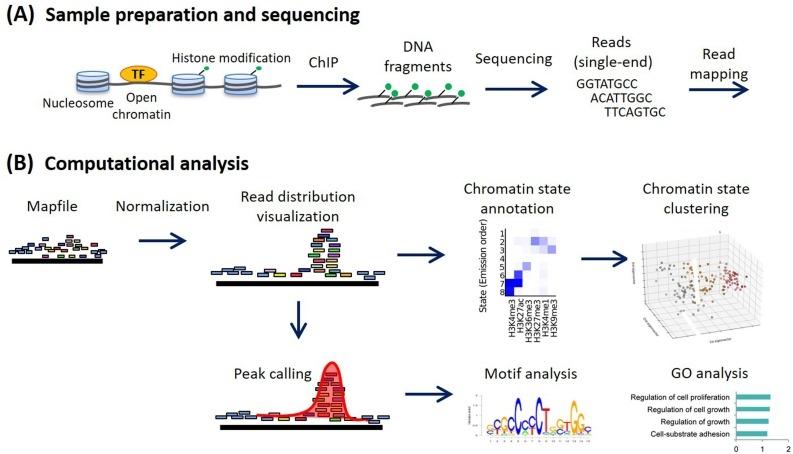
Methoden voor ChIP-seq-analyse: Een praktische workflow en geavanceerde toepassingen - ScienceDirect
1) Definieer "Laag signaal" Voordat je iets verandert
Laag signaal kan verschillende dingen betekenen: te weinig pieken, zwakke verrijking bij bekende loci, of een bibliotheek die er prima uitziet maar slecht in kaart is. Goede ChIP-Seq probleemoplossing begint met het duidelijk labelen van de faalmodus, omdat elke modus naar verschillende oplossingen wijst.
Een beginnersvriendelijke manier om het probleem te definiëren is door drie lagen te controleren:
✓ Biologielaag: Is het doelwit aanwezig in je celtoestand (gestimuleerd versus rustend, differentiatiefase, behandeltijd)?
✓ Verrijkingslaag: Toont ChIP-DNA verrijking door qPCR op een positieve controlelocus versus een negatieve regio?
✓ Sequencing-laag: Heb je genoeg unieke, toegewezen reads en een redelijk duplicaat niveau?
Als je deze drie niet kunt beantwoorden, "optimaliseer dan niet alles." Voer eerst één gecontroleerd experiment uit: houd het monster hetzelfde, houd de sequencingdiepte bescheiden en verander slechts één vermoedelijke variabele.
2) Begin met chromatine: fragmentgrootte eenen verliesbeheersing
Wanneer laboratoria vragen waarom een ChIP "niet werkt", is de meest voorkomende oorzaak chromatine die overgefragmenteerd, ondergefragmenteerd of simpelweg verloren gaat tijdens het schoonmaken. Bij ChIP-Seq Troubleshooting is chromatine je basis – als het inconsistent is, wordt elke latere stap ruis.
Voor op sonicatie gebaseerde workflows mikken veel laboratoria op fragmenten in het ~150–300 bp-bereik voor scherpe piekroep en consistente immunoprecipitatie. Als fragmenten meestal groter zijn (bijvoorbeeld >500 bp), hebben antistoffen moeite om doelcomplexen efficiënt naar beneden te trekken. Als fragmenten te klein zijn, kun je epitopen vernietigen of achtergrond vergroten door niet-specifiek DNA vrij te geven.
Praktische controleposten die je direct kunt doen:
• DNA meten na reverse crosslink en cleanup (niet alleen vóór IP). Een grote daling hier duidt op verlies van kralen/kolommen of harde omstandigheden.
• Fragmentatieprofielen over monsters vergelijken. Als één monster "perfect" is en het volgende uitgesmeerd of te groot is, focus dan eerst op lysis- en sonicatie-instellingen, niet op antistoffen.
• Bewaar een "input DNA" aliquot van elke batch. Dit is je basislijn voor zowel qPCR als bibliotheekcontrole.
Bij Longlight Technology raden we aan om chromatinevoorbereiding te behandelen als een gecontroleerde productiestap: de buffersamenstelling vaststellen, de temperatuur van het monster stabiel houden tijdens de sonicatie en de exacte cyclusinstellingen registreren. Kleine afwijkingen zorgen later voor grote verschillen in pieksterkte.
3) Antilichaampasvorm: specificiteit, partijvariatie, eennd Controles
Als chromatine redelijk lijkt, is de volgende stap in ChIP-Seq Troubleshooting het selecteren en valideren van antistoffen. Een laag signaal wordt vaak veroorzaakt door het gebruik van een antilichaam dat "goed is voor het westers" maar zwak voor ChIP, of door lot-tot-lot-variabiliteit.
Een goede antistofstrategie is opgebouwd rond controles:
✓ Positief controledoel: een histonmarkering met robuuste verrijking (vaak gebruikt om de gezondheid van de workflow te bevestigen).
✓ Negatieve controle: IgG of een isotypecontrole om achtergrondpull-down te schatten.
✓ Bekende loci qPCR: één of twee gepubliceerde positieve loci voor je doelwit, plus een genwoestijnregio.
Voor transcriptiefactoren kan het signaal inherent lager zijn dan histonenmarkeringen. Dat betekent dat je antilichaam een hoge affiniteit moet hebben en je IP-condities schoon moeten zijn. Als je nieuw bent met TF ChIP, begin dan niet met het veranderen van de sequencing-diepte. Bevestig eerst verrijking met qPCR. Als de qPCR-verrijking zwak is, zullen meer reads meestal meer ruis veroorzaken.
Praktische tip: Wanneer je van antistofbatch wisselt, controleer indien mogelijk de verrijking op dezelfde chromatinebatch opnieuw. Als de kavelwijziging het signaal breekt, is de workflow niet per se "fout"—je reagensprestaties zijn veranderd, en je probleemoplossingspad zou dat moeten weerspiegelen.
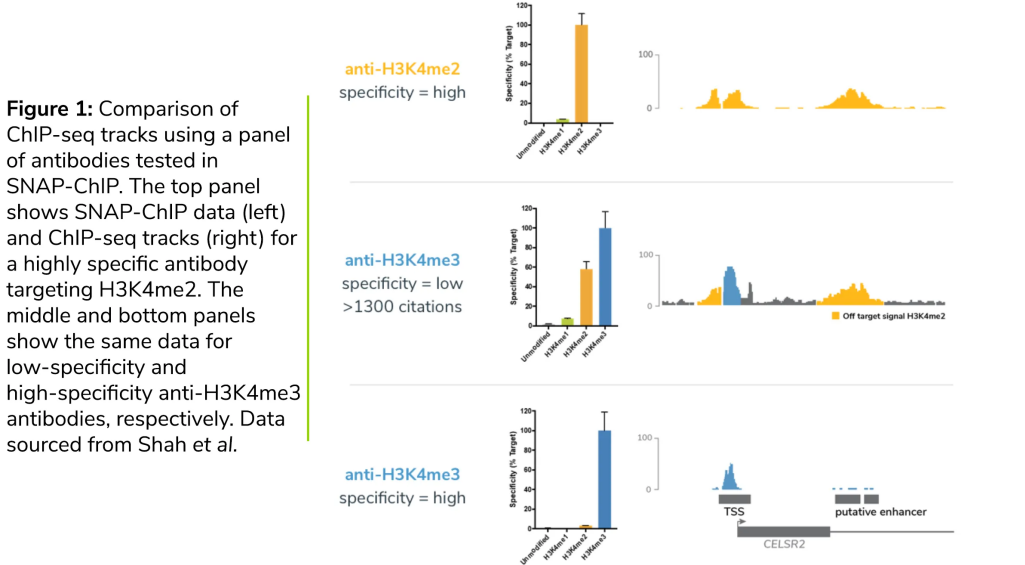
Het juiste ChIP-antilichaam kiezen voor uw experiment - EpiCypher
4) Schone IP-optimalisatiesequentie—Geen giswerk
Naast chromatine en antistoffen is IP-chemie (kralen, washes, incubatie) de volgende hotspot. Laag signaal is vaak een achtergrondprobleem.
✓ Kralenselectie: Kies Eiwit A/G dat past bij jouw antilichaamsoort/isotype.
✓ Hoeveelheid antistoffen: Titreer om zwakke pull-down of verhoogde niet-specifieke DNA te voorkomen.
✓ Washbalans: Kalibreer strengheid om ruis te verwijderen maar zwakke maar reële interacties te behouden.
Een praktische beginnersregel is om per run slechts één as aan te passen:
• Als er pieken zijn maar zwak zijn, verhoog de effectieve vangst (iets meer antilichaam, verbeterde kraalbinding, langere incubatie).
• Als pieken breed en ruiserig zijn, verhoog de specificiteit (sterkere washes, betere blokkade, verminder antistofoverbelasting).
Vanuit het perspectief van de fabrikant ontwerpt Longlight Technology immunoprecipitatiereagentia en magnetische parelsystemen om verlies tijdens het hanteren te minimaliseren, omdat monsterverlies precies lijkt op "laag signaal." Gladde parelscheiding, consistente binding en schone wasstappen verminderen de variabiliteit tussen operators—vooral belangrijk voor teams die nieuw personeel opleiden.
5) Bibliotheekcontrole: Wanneer "Goed DNA" Geeft nog steeds een laag signaal
Soms is ChIP DNA-verrijking echt, maar de uiteindelijke data ziet er nog steeds vlak uit. Bij ChIP-Seq Troubleshooting wijst dit meestal op bibliotheekconstructie of sequencing-metrics.
Veelvoorkomende oorzaken van een laag signaal op bibliotheekniveau:
✓ Overversterking: te veel PCR-cycli kunnen duplicaten opblazen en bruikbare unieke reads verminderen.
✓ Adapter/primer-artefacten: deze verbruiken sequencing reads zonder de doeldekking te verbeteren.
✓ Slechte complexiteit: vaak veroorzaakt door zeer weinig ChIP DNA-invoer of verlies tijdens het schoonmaken.
Wat je moet controleren voordat je de hele ChIP opnieuw uitvoert:
• Bibliotheekgrootte distributie (je wilt een schone piek, niet meerdere onverwachte pieken).
• Duplicaatsnelheid en unieke mappingsnelheid na uitlijning.
• De trend van het percentage reads in peaks (FRiP) ten opzichte van je interne basislijn (zelfs beginners kunnen "beter versus slechter" volgen over runs heen).
Als je library overcycling vermoedt, is een eenvoudige verbetering het verminderen van het aantal cyclen en het verhogen van de capture-efficiëntie stroomopwaarts (betere chromatineherstel en IP-specificiteit). Dieper sequencen kan niet compenseren voor een bibliotheek met lage complexiteit.
6) Stap-Bij-Step Signal Recovery Je kunt morgen beginnen
Een praktische sequentie die beter presteert dan ad-hoc tweaken:
✓ Stap 1: Controleer of chromatinefragmenten ~150–300 bp zijn en bevestig DNA-herstel na reverse crosslink.
✓ Stap 2: Controleer verrijking met qPCR op één positieve en één negatieve locus vóór de bibliotheekvoorbereiding.
✓ Stap 3: Voeg de juiste bedieningselementen toe (invoer IgG) om "geen verrijking" te scheiden van "hoge achtergrond".
✓ Stap 4: Stel de IP-condities één variabele tegelijk af (kralen, hoeveelheid antistoffen, wasstringentie).
✓ Stap 5: Controleer bibliotheekstatistieken (duplicatie, mapping, grootteverdeling) voordat je aanneemt dat sequencing depth het probleem is.
CTA (Longlight Technologie): Als je een snellere route wilt, neem dan contact op met Longlight Technology voor een ChIP-Seq probleemoplossingschecklist en een voorbeeld-voor-sample diagnostisch werkblad (chromatine → IP → library). We kunnen ook een strategie voor het ontwerp van besturing en reagentiakoppeling aanbevelen om de variabiliteit van operators te verminderen en beginners te helpen sneller stabiele verrijking te bereiken.
Een zwak signaal is frustrerend, maar zelden mysterieus. Met een gedisciplineerde ChIP-Seq probleemoplossingsflow—beginnend bij chromatineintegriteit, vervolgens antilichaampasvorm, vervolgens IP-specificiteit, en tenslotte bibliotheekcontrole—kun je één zwakke run omzetten in een herhaalbaar protocol dat schaalt over samples, personeel en projecten.