Gerelateerd artikel
ChIP: Onthullen hoe eiwitten genen beheersen: Begint met één eenvoudige vraag
2026-02-25ChIP: Onthullen Hoe eiwitten genen reguleren is de praktische methode die wetenschappers gebruiken om een vraag te beantwoorden die centraal staat in de moderne biologie: welke eiwitten zitten op welke DNA-gebieden, in echte cellen, onder echte omstandigheden? Als je nieuw bent in genregulatie, helpt het om DNA te zien als een bibliotheek en regulerende eiwitten als "lezers" die specifieke pagina's op bepaalde tijden openen. ChIP (chromatine immunoprecipitation) is hoe we dat moment vastleggen en de pagina's identificeren.
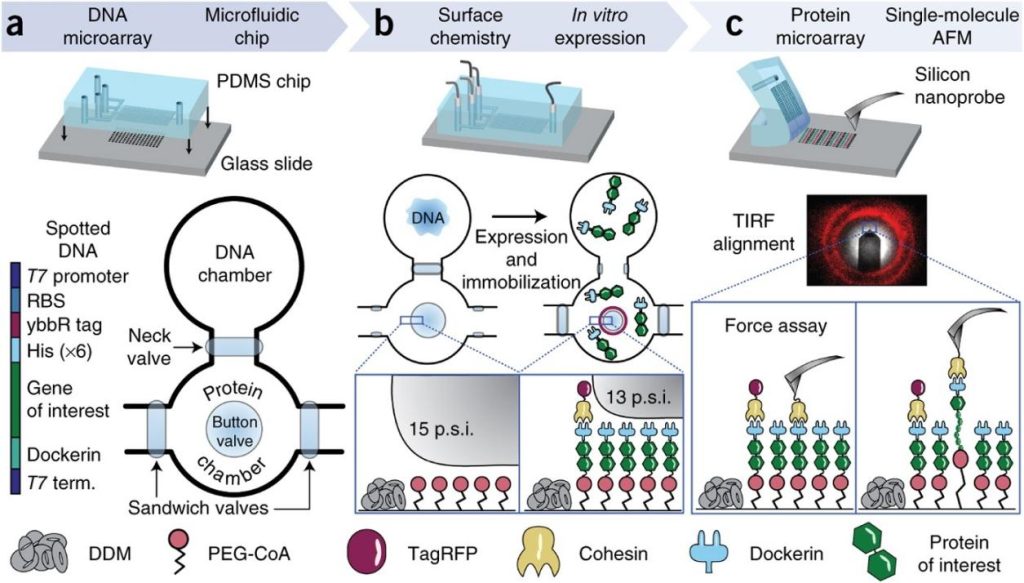
Van genen tot eiwitmechanica op een chip | Nature Methods
Bij Longlight Technology produceren en ondersteunen we kernworkflowtools die worden gebruikt in chromatineonderzoek—van essentiële monsterbehandelingen tot verrijking en downstream detectieopties—zodat nieuwe teams kunnen beginnen met een schoon, herhaalbaar traject en ervaren teams met vertrouwen kunnen opschalen.
Wat ChIP daadwerkelijk meet en waarom het belangrijk is
In eenvoudige termen, Bikken test of een eiwit fysiek geassocieerd is met een specifiek DNA-gebied binnen de cel. Het wordt veel gebruikt voor transcriptiefactoren, co-factoren en histonmodificaties, omdat dit de "schakelaars" zijn die bepalen of genen actief, gepauzeerd of stil zijn. Een standaard ChIP-workflow omvat meestal crosslinking (voor veel doelwitten), chromatinefragmentatie, antilichaam-gebaseerde verrijking, DNA-zuivering en uitlezen via qPCR (targeted) of sequencing (genoombreed).
Daarom is ChIP: Revealing How Proteins Control Genes meer dan een laboratoriumtechniek—het is een beslissingsinstrument. Het helpt onderzoekers:
✓ Bevestig of een vermoedelijke regulator een promotor of versterker bindt
✓ Vergelijk bindingsveranderingen vóór/na behandeling of stress
✓ Kaarthistonmarkeringen die correleren met actieve of onderdrukte chromatinetoestanden
✓ Bewijs opbouwen voor mechanismen in epigenetica, oncologie, immunologie en ontwikkeling
De kernworkflow in zes stappen
De meeste beginners slagen sneller als ze ChIP behandelen als een keten van "moet-niet-doorbreken"-stappen, niet als één enkel experiment. Hier is de praktische volgorde achter ChIP: Hoe eiwitten genen reguleren:
• Fix (optioneel maar gebruikelijk): Veel ChIP-protocollen gebruiken omkeerbare crosslinking, vaak met 1% formaldehyde gedurende ~10 minuten, gevolgd door afkoeling (vaak met glycine).
• Lysis/chromatine voorbereiding: Standaardiseer kernen/chromatine voor consistentie.
• DNA-afschuiving: Fragmentatie regelt resolutie en verrijkingssnelheid.
• Immunoprecipitatie: Antistofspecificiteit is de primaire bepalende factor van S/N.
• Cross-link reversal (indien gebruikt) en DNA-zuivering: Hogere zuiverheid verhoogt de gevoeligheid van de assay.
• Lees voor: Gebruik ChIP-qPCR voor gerichte vragen, of ChIP-seq voor genoombrede mapping.
Longlight Technology CTA: Als je je eerste ChIP-workflow opzet, neem dan contact op met ons team voor een checklist van begin tot eind (sample-to-data) die is gekoppeld aan je doeltype (TF versus histonmarkering) en je readoutplan (qPCR vs sequencing).
Fragmentatie en kruisverbinding: De twee settings die je uitkomst bepalen
Als je ChIP-resultaten "willekeurig" aanvoelen, ligt de oorzaak vaak stroomopwaarts. Twee settings domineren reproduceerbaarheid:
Crosslinking, kracht en tijd. Zware crosslinking kan zwakke interacties stabiliseren, maar het kan ook de DNA-opbrengst verminderen en de stappen later bemoeilijken. Veel standaardprotocollen vermelden 1% formaldehyde met korte incubatievensters bij kamertemperatuur, zoals ~10–15 minuten, gevolgd door afkoeling.
Fragmentgrootte. Voor de meeste ChIP-toepassingen wordt een vaak aanbevolen afschuifbereik van ~200–600 bp, wat de resolutie in balans brengt met herstelbaarheid tussen celtypen en weefsels.
✓ Te groot (bijvoorbeeld >800–1000 bp) verlaagt vaak de resolutie en vergroot de achtergrond
✓ Te klein kan epitopen beschadigen, lager herstelbaar DNA of biasbibliotheken veroorzaken
✓ De "beste" instellingen zijn afhankelijk van het instrument en de sample, dus optimalisatie is normaal, geen mislukking
Dit is de verborgen waarheid achter ChIP: Onthullen Hoe Eiwitten Genen Reguleren: de schoonste downstreamanalyse kan inconsistente chromatine-bereiding niet redden.
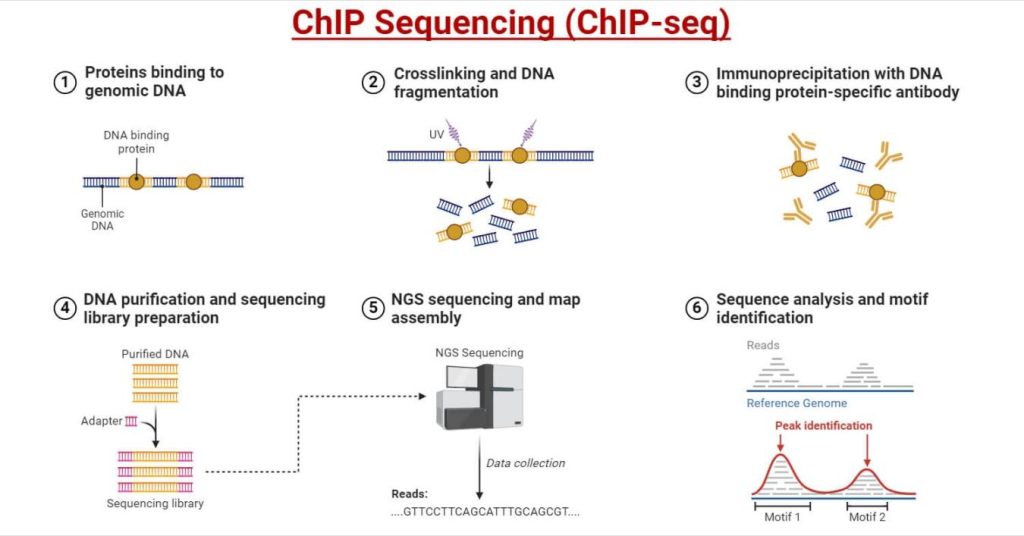
ChIP-sequencing (ChIP-seq): Principe, stappen, toepassingen, diagram
Antistoffen, controles en hoe "goede verrijking" eruitziet
ChIP is een antilichaam-gedreven assay, dus je doelantilichaam en je controles bepalen of je data vertrouwd zal worden.
Maatregelen die je vanaf dag één moet plannen:
✓ Voer DNA in (een fractie chromatine vóór IP) om herstel te normaliseren
✓ IgG-controle om niet-specifieke pull-down achtergrond te meten
✓ Een bekende positieve locus (indien beschikbaar) om te bevestigen dat het systeem werkt
Realistische verwachtingen van verrijking verschillen per doeltype. Sommige aanbieders melden bijvoorbeeld dat transcriptiefactor/co-factor ChIP-verrijkingen zo laag kunnen zijn als ~0,5% van de totale input, terwijl histonmodificatie ChIP dramatisch hoger kan zijn (tientallen procent) afhankelijk van markabundantie en antistofprestaties; typische IgG-achtergrond met kralen kan ongeveer ~0,05–0,1% van de input zijn.
Die range is niet bedoeld om je te intimideren—het is bedoeld om je te beschermen tegen valse verwachtingen. In ChIP: Onthullen Hoe Eiwitten Genen beheersen, kan "klein" nog steeds correct zijn, zolang het specifiek, reproduceerbaar en boven de juiste controle staat.
Longlight Technology CTA: Als je problemen zoekt met hoge achtergrond- of zwakke signalen, vraag ons dan om een sjabloon voor regelontwerp (primerstrategie, input fraction planning en achtergronddrempels) zodat je de bottleneck snel kunt diagnosticeren.
ChIP-qPCR versus ChIP-seq: Het juiste uitlezen kiezen voor uw doel
Een beginnersvriendelijke regel is: qPCR antwoordt "Is het daar?" terwijl sequencing antwoordt "Waar is het nog meer?"
ChIP-qPCR is ideaal als je een kleine set vermoedelijke regio's hebt (promotors/enhancers) en je snelle iteratie nodig hebt. Het is ook een praktische opstapje voordat je investeert in sequencing.
ChIP-seq is de keuze voor ontdekking en genome-brede mapping, maar vereist planning voor diepte- en kwaliteitsindicatoren. ENCODE-richtlijnen bieden veelvoorkomende doelen zoals:
Voor transcriptiefactor-/narrow-peak-experimenten: minimaal ~10 miljoen bruikbare fragmenten per replicate, met hogere aanbevolen doelen.
Voor brede histonenmarkeringen: minimaal ~20 miljoen bruikbare fragmenten per replicate, met hogere aanbevolen doelen afhankelijk van de doelen.
Deze cijfers zijn niet zomaar "sequencing-advies." Ze bepalen hoeveel startmateriaal je nodig hebt, hoe streng je antilichaam moet zijn en hoe zorgvuldig je batch-effecten moet beheren. Daarom wordt ChIP: Revealing How Proteins Control Genes vaak gewonnen of verloren in de ontwerpfase.
Qubit assay tubes en ChIP-Seq Service Advantage: Eén workflow, één standaard
Van voorbeeld tot rapport
Om ChIP: Onthulling Hoe eiwitten genen reguleren praktisch te maken voor echte onderzoekstijden, moet de workflow consistent blijven van monsterinname tot definitieve interpretatie. Longlight Technology combineert betrouwbare verbruiksmaterialen—zoals Qubit Assay Tubes—met een end-to-end ChIP-seq-dienst die is ontworpen om overdrachten te verminderen, variabiliteit te beheersen en resultaten gemakkelijk te interpreteren voor zowel beginners als ervaren teams.
One-stop-service die knelpunten wegneemt
Ons servicemodel is ontworpen voor labs die ChIP-seq resultaten willen bereiken zonder zelf een volledige sequencing-pijplijn te bouwen. Je levert vaste celmonsters of bevroren weefselmonsters, en we voltooien de resterende stappen met gestandaardiseerde controlepunten:
✓ Monstervoorbereiding en acceptatiekwaliteitscontrole
✓ Chromatineafschuiving en fragmentatiecontrole
✓ Bibliotheekbouw en bibliotheekcontrole
✓ On-instrument sequencing en data-QC
✓ Bio-informatica Analyse en gestructureerde rapportage
✓ Levering van volledige rapporten en ruwe data
Strenge kwaliteitscontrole bij elke link
ChIP-seq is afhankelijk van signaal-ruisprestaties. Subtiele procesvariatie in hantering, afschuif of bibliotheekmetrieken kan het ware signaal verdunnen. Longlight Technology implementeert strakke kwaliteitscontroles overal om vertrouwde verrijking en duidelijke binding te interpreteren.
✓ Stapsgewijze kwaliteitscontrole om reproduceerbaarheid te beschermen
✓ Datakwaliteitscontroles die experimentele kwaliteitscontrole afstemmen op downstreamanalyse
✓ Schone rapportage die je helpt binding te lokaliseren bij specifieke genen of regio's met meer vertrouwen
Geschikt voor kleine steekproefgroottes
Veel onderzoeksteams werken met beperkt materiaal, vooral bij het bestuderen van primaire cellen, zeldzame weefsels of monsters in een vroeg stadium. Onze geoptimaliseerde experimentele flow is ontworpen om ChIP-seq experimenten en analyses uit te voeren, zelfs wanneer de steekproefinvoer beperkt is.
✓ Procesoptimalisatie voor projecten met lage input
✓ Praktische ontwerprichtlijnen om "herwerkslussen" veroorzaakt door onvoldoende kwaliteitscontrole te vermijden
✓ Stabiele workflow om kleine steekproefstudies interpreteerbaar te houden
Gerichte vragen: Specifieke genen of regio's, of genoombrede ontdekking
ChIP bestudeert eiwit–DNA-interacties op een manier die de echte chromatinecontext weerspiegelt. ChIP-seq combineert ChIP met next-generation sequencing om DNA-locaties te detecteren die gebonden zijn aan specifieke transcriptiefactoren of histonen in het genoom. Afhankelijk van uw doel kan onze analyse zowel gericht als ontdekkingsgedreven werk ondersteunen.
ChIP-seq kan u helpen vragen te beantwoorden zoals:
✓ Vergelijk waar een eiwit zich bevindt tussen locaties en kaart binding in een doelgenomisch gebied in kaart
✓ Ontdek hoe histonmodificatiepatronen zich verhouden tot veranderingen in genexpressie
✓ Identificeer de precieze positionering van RNA-polymerase II en andere transfactorbindingsplaatsen
✓ Bestudeer transcriptiefactoren om binding te verbinden met regulatorische uitkomsten
Waarom kiezen voor Longlight-technologie
Longlight Technology ondersteunt moderne genomica met een praktisch product- en service-ecosysteem. Naast ChIP-seq-diensten bieden wij NGS-gerelateerde instrumenten zoals Focused Ultrasonicator, plus hoogwaardige reagentia en verbruiksartikelen die worden gebruikt in academische, klinische en industriële omgevingen.
✓ Consumables And Kits: prefab agarosegels, nucleïnezuur-aaseren, qubitbuizen, nucleïnezuurextractiekits en bibliotheekvoorbereidingskits
✓ Genomics Solutions: producten ontworpen om de efficiëntie, nauwkeurigheid en herhaalbaarheid van het laboratorium te verbeteren
✓ Research Support: workflow-begeleiding die teams helpt van voorbeelden naar bruikbare conclusies te gaan
Laatste conclusie
ChIP: Onthullen Hoe eiwitten genen reguleren werkt het beste als je het behandelt als een gecontroleerd systeem: stabiele chromatinevoorbereiding, gevalideerde antilichamen, eerlijke controles en een uitlezing die aansluit bij je vraag zelf. Als je de workflow met die logica bouwt, wordt ChIP een van de duidelijkste vensters naar genregulatie die je in een modern laboratorium kunt gebruiken.
Als je wilt, deel dan je doeltype (TF versus histonmarkering) en voorbeeldformaat (cellen versus weefsel), en ik kan een beginnersvriendelijke workflowchecklist en kwaliteitscontrolepunten uitwerken die passen bij jouw gebruikssituatie—nog steeds in dezelfde duidelijke, leesbare stijl.